- Definition: Was ist ein Hodenhochstand?
- Häufigkeit des Hodenhochstandes
- Risikofaktoren für einen Hodenhochstand
- Mögliche Auswirkungen und Langzeitschäden eines Hodenstands
- Wie wird ein Hodenhochstand diagnostiziert?
- Therapie beim Hodenhochstand
- Komplikationen bei der operativen Therapie des Hodenhochstandes
- Schlussfolgerung zum Hodenhochstand
Als Hodenhochstand wird ein ausgebliebener bzw. unvollständiger Abstieg des Hodens in den Hodensack bezeichnet. Der Hodenhochstand tritt bei etwa 2 bis 4 Prozent aller neugeborenen Jungen auf und ist damit die häufigste männliche Genitalfehlbildung. Die operative Fixierung des Hodensacks im Rahmen einer Orchidopexie stellt das entscheidende Therapieverfahren zur Behandlung eines Hodenhochstands dar.
Definition: Was ist ein Hodenhochstand?
Der Hodenhochstand bezeichnet die fehlende Absenkung (Deszensus) eines oder beider Hoden in den Hodensack (Skrotum) und stellt mit 2 bis 4 Prozent aller Reifgeborenen die häufigste angeborene (kongenitale) Fehlbildung der Knaben dar. Trotz seiner milden Präsentation kann der Hodenhochstand die männliche Gesundheit erheblich beeinträchtigen und umfangreiche medizinische und ökonomische Ressourcen fordern. Denn der Hodenhochstand stellt den einzigen anerkannten Risikofaktor für einen Hodentumor dar und kompromittiert häufig die spätere Fertilität. Unklare Definitionen und widersprüchliche Ergebnisse der Literatur machen seine Behandlung dabei zu einem vieldiskutierten Thema. Praktische Empfehlungen auf der Grundlage evidenzbasierter Daten zur Behandlung des präpubertären Hodenhochstandes werden in diesem Beitrag gegeben.
Häufigkeit des Hodenhochstandes
Bei der Geburt weisen 2,5 bis 4 Prozent aller neugeborenen Knaben einen Hodenhochstand auf, wobei deutliche, aber ungeklärte geographische Unterschiede bestehen. Die sog. Prävalenz (Krankheitshäufigkeit) beträgt im 3. Lebensmonat 1 bis 1,9 Prozent und im 18. Monat 0,8 bis 1,5 Prozent. Eine häufig vermutete Zunahme der Häufigkeit konnte nicht bestätigt werden. Auffallend ist eine höhere Operationsfrequenz als aufgrund der Prävalenzdaten zu erwarten ist. Dies weist darauf hin, dass zu viele Pendelhoden operiert werden.
Risikofaktoren für einen Hodenhochstand
Zu den Risikofaktoren, die einen Hodenhochstand begünstigen können, gehören:
- eine genetische Disposition
- ein niedriges Geburtsgewicht
- eine pränatale Exposition gegenüber Hormonabbruchpräparaten („Pille“)
- eine pränatale Exposition gegenüber Nikotin bei beiden Elternteilen
Mögliche Auswirkungen und Langzeitschäden eines Hodenstands
Risiko einer Fertilitätsstörung beim Hodenstand
Männer mit einem in der Kindheit behandelten Hodenhochstand weisen eine reduzierte Fertilitätschance aufgrund schlechterer Spermienqualität auf. Das Risiko für Subfertilität (eingeschränkte Zeugungsfähigkeit) steigt bei einer beidseitigen Fehllage der Gonade (Keim- oder Geschlechtsdrüse; beim Mann der Hoden) und einem Behandlungsbeginn nach der ersten Lebensdekade, wird jedoch nicht durch einen normal deszendierten (aus der Bauchhöhle herabgewanderten) kontralateralen (auf der entgegengesetzten Körperseite oder -hälfte gelegenen) Hoden kompensiert. Erwachsene Männer mit einem unbehandelten beidseitigen Kryptorchismus (das Fehlen beider Hoden im Hodensack) besitzen ein sehr hohes Sterilitätsrisiko. Nach operativer Korrektur sinkt dieses Risiko auf 38 Prozent in Vaterschaftsstudien, wobei keine Korrelation zum Alter der behandelten Patienten angegeben wird. Die Hodenlage vor Therapiebeginn soll keinen Einfluss auf die Fertilität haben.
Die Zeugungsraten der erfolgreich wegen eines einseitigen Hodenhochstandes behandelten Patienten sind nur gering vermindert. Unfruchtbarkeit wurde nur bei 10 Prozent der Betroffenen im Gegensatz zu 6 Prozent bei normalen Kontrollpersonen nachgewiesen. Es fehlen jedoch Studien, welche die Fertilität behandelter mit der unbehandelter Männer bei einseitiger Gonadenfehllage vergleichen. Allerdings wird die Vaterschaftsrate weder durch eine einseitige Hodenagenesie (angeborenes Fehlen der Hoden durch Nichtanlage) noch eine einseitige Hodenentfernung beeinflusst.
Möglichst früher Behandlungsbeginn wirkt sich günstig aus
Ein junges Alter zum Operationszeitpunkt korreliert mit günstigen FSH- und Inhibin B-Spiegeln im höheren Lebensalter. Ob dies allerdings einen positiven Einfluss auf die spätere Fertilität hat, ist unbekannt. Jedoch lassen sich morphologische Veränderungen bereits im 9. Lebensmonat nachweisen. Jüngste Daten weisen auf eine Keimzellschädigung nur nach dem 12. Lebensmonat hin. Das längere extraskrotale (außerhalb des Hodensacks) Verweilen einer Gonade ist assoziiert mit einer progressiven testikulären Fibroserate (krankhafte Vermehrung des Bindegewebes im Hoden) und dem vermehrten Auftreten einer Leydigzelldysplasie. Zudem besteht bei nicht palpablen (tastbarem) Hoden im Gegensatz zu tastbaren ein 50 Prozent höheres Risiko eines Keimzellverlustes. Diese Tatsachen bilden die Grundlage für die Forderung nach einem frühen Behandlungsbeginn beim Hodehhochstand zwecks Prävention von Langzeitschäden. Das Hodenwachstum wird durch eine Operation mit 9 Monaten stärker gefördert als im Alter von 3 Jahren.
Schließlich gibt es einen weiteren, zu wenig beachteten Grund für eine postpubertäre Fertilitätsstörung: Fehlbildungen des Nebenhodens und der Samenwege (Abbildung 1). Diese Dysgenesien (Fehlentwicklungen) finden sich in 35 bis 90 Prozent aller dystopen (an der falschen Stelle gelegenen) Hoden, während sie bei orthotoper (an der richtigen Stelle gelegenen) Hoden nur in 5 Prozent nachweisbar sind. Deshalb ist der Erhalt der Hodenfunktion unabhängig vom Alter irrelevant, wenn die speichernden und ableitenden Samenwege funktionsuntüchtig sind.
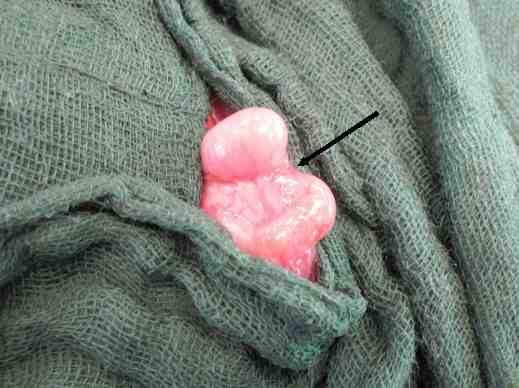
Abbildung 1: Fehlbildungen der Samenwege: Hoden-Nebenhoden-Dissoziation (Pfeil)
Risiko eines Hodentumors beim Hodenhochstand
Das relative Risiko eines nach der Pubertät auftretenden Hodentumors (Hodenkrebs) ist bei Patienten mit einem Hodenhochstand 5mal höher als in der Allgemeinbevölkerung. 10 Prozent aller bösartigen Hodentumoren sind mit einer Hodenfehllage assoziiert. Bei einer Behandlung vor dem 10. Lebensjahr besteht allerdings nur ein doppelt so hohes Risiko im Vergleich zu Gesunden.
Hodentumoren entwickeln sich aus präinvasiven Läsionen, dem Carcinoma in situ (CIS) oder der testikulären intraepithelialen Neoplasie (TIN). Eine systematische Hodenbiopsie zum Zeitpunkt der Orchidopexie (Hodenoperation) ist jedoch zur frühzeitigen histologischen Suche nach malignen (bösartigen) oder prämalignen Zellen nicht erforderlich. Das Risiko für die Entstehung eines Hodentumors ist bei einem beidseitigen Hodenhochstand höher als bei einem einseitigen. Die Anleitung der Eltern und später der Betroffenen zur Selbstuntersuchung erhöht die Möglichkeit einer Frühdiagnose.
Für die sehr seltenen präpubertären testikulären Neoplasien, die im Gegensatz zur jugendlichen und erwachsenen Population eine unterschiedliche Tumorbiologie aufweisen, stellt der Hodenhochstand keinen Risikofaktor dar.
Risiko einer psychosexuellen Beeinträchtigung beim Hodenhochstand
Eine Hodenfehllage bzw. ein Hodenhochstand kann die psychosexuelle Entwicklung beeinträchtigen. Die Spermarche (Beginn der Spermienproduktion in den Hoden) findet zwar später statt, jedoch sind Penisgröße, Testosteronspiegel, Potenzprobleme und männliche Identitätsangaben vergleichbar mit der Allgemeinbevölkerung. Die Literatur zur Rolle des an normaler Stelle gelegenen Hodens bei neurotischen Störungen ist leider sehr spärlich.
Risiko einer Hodentorsion beim Hodenhochstand
Trotz weitverbreiteter Ansicht gibt es keine gesicherten Daten, die auf ein erhöhtes Risiko für eine Hodentorsion (partielle oder totale Drehung des Hodens um den versorgenden Gefäßstiel) hinweisen.
Wie wird ein Hodenhochstand diagnostiziert?
Körperliche Untersuchung zur Diagnose eines Hodenhochstandes
Die Diagnose eines Hodenhochstandes wird klinisch gestellt. Sie sollte durch einen erfahrenen Untersucher in warmer, entspannter Umgebung gestellt werden, um den Kremasterreflex (Hodenheber-Reflex durch Bestreichung der Innenseite des Oberschenkels) zu minimieren. Dabei ist im Schneidersitz ein Ausstreichen des Leistenkanals mit dem Versuch der Palpation (Betastung) des Hodens sinnvoll (Abbildung 2).
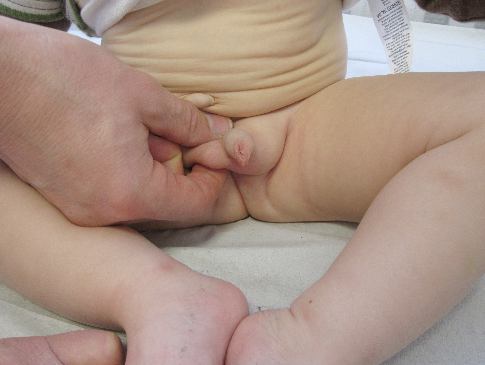
Abbildung 2: Untersuchung in warmer, entspannter Umgebung im Schneidersitz
Die folgende Abbildung (Abbildung 3) zeigt die unterschiedlichen Lokalisationen des Hodens aufgrund der körperlichen Untersuchung.
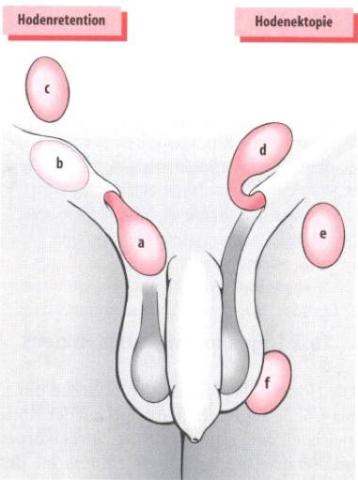
Abbildung 3: Unterschiedliche Hodenlokalisationen
Wichtig ist im klinischen Alltag die exakte Abgrenzung zwischen Gleit- und Pendelhoden, da beide Formen nicht immer sicher voneinander abgegrenzt und zu häufig nur kontrollbedürftige Pendelhoden behandelt werden. Gleithoden sind durch einen kurzen Samenstrang gekennzeichnet. Die Gonade lässt sich zwar in den Hoden verlagern, zieht sich jedoch beim Loslassen wieder in die Leiste zurück. Im Gegensatz hierzu weist der Pendelhoden einen ausreichend langen Samenstrang auf, so dass die Gonade nach skrotaler Positionierung im Hodensack verbleibt. Erst nach Auslösen des Kremasterreflexes kommt es zum Hodenaufstieg.
Ein spontaner Hodenabstieg kann nur bis zum 6. Lebensmonat erwartet werden. Die Hodenlokalisation sollte schriftlich in den pädiatrischen Untersuchungsheften dokumentiert werden, um einen in bis zu 20 Prozent aller heruntergewanderten Hoden vorkommenden sekundären Hodenhochstand entdecken zu können.
Labordiagnostik zur Diagnose eines Hodenhochstandes
Beidseits nicht tastbare Hoden, vergesellschaftet mit einer Hypospadie (Harnröhrenfehlbildung), lassen eine sexuelle Differenzierungsstörung vermuten und erfordern eine hormonelle und genetische Abklärung. Dabei muss ein weiblicher Karyotyp mit assoziiertem adrenogenitalen Syndrom ausgeschlossen werden. Ein beidseitiger nicht tastbarer Hoden ohne Hypospadie erfordert einen HCG-Test zum Nachweis der Existenz funktionstüchtigen Hodengewebes (Abbildung 4). Bei einer Anorchie (fehlende Hoden) bleibt ein Testosteronanstieg nach HCG-Gabe aus und es finden sich zudem erhöhte FSH- und LH-Werte.
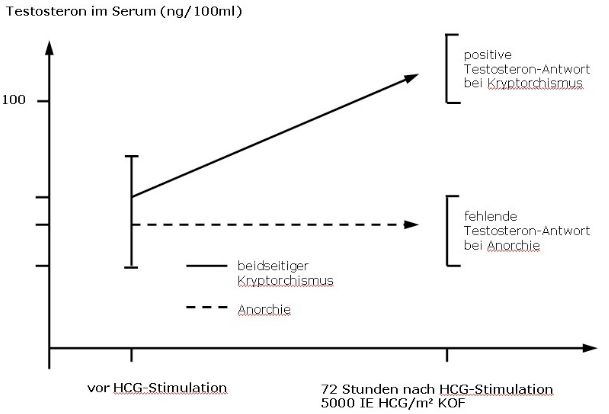
Abbildung 4: HCG-Test beim bilateralen Kryptorchismus: 72 Stdunden nach HCG-Gabe Testosteron-Anstieg nur bei Bauchhoden
Alternativ kann bei nicht tastbaren Hoden eine Inhibin-B-Bestimmung erfolgen. Dieses Peptidhormon wird präpubertär nur von den Sertoli-Zellen des Hodens sezerniert. Ein positiver Wert weist ein vorhandenes testikuläres Parenchym nach, ein fehlender Nachweis dokumentiert fehlendes Hodengewebe.
Bildgebung und Laparoskopie zur Diagnose eines Hodenhochstandes
Bei nicht tastbarem Hoden erlaubt die Sonografie mit hochauflösendem Schallkopf (>7,5 MHz) nur eine korrekte Klassifikation in 84 Prozent der Fälle. Das zuverlässigste Verfahren stellt die Laparoskopie (Bauchspiegelung) dar, die nicht nur eine exakte Bauchhoden-Diagnostik (Abbildung 5), sondern auch eine gleichzeitige Behandlung bei normal entwickeltem Hoden ermöglicht.
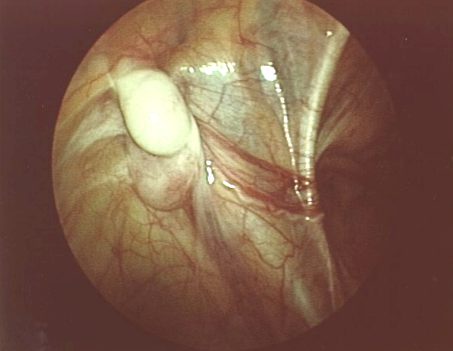
Abbildung 5: Diagnostische Laparoskopie: Erhaltenswerter Bauchhoden (mit freundlicher Genehmigung von Prof. Rösch, Regensburg)
Therapie beim Hodenhochstand
Im ersten Lebenshalbjahr kann ein spontaner Hodenabstieg abgewartet werden. Die Behandlung sollte im 6. Lebensmonat beginnen und am 1. Geburtstag abgeschlossen sein. In einer randomisierten, kontrollierten Studie ergab sich bei früher Operation im 9. Monat ein besseres postoperatives Hodenwachstum als in der Kontrollgruppe und bei einer Intervention im 3. Lebensjahr. Die Spermiengesamtzahl und -beweglichkeit war in einer anderen Studie trotz kleiner Fallzahlen signifikant besser bei früher Operation im 1. Lebensjahr als bei einem Eingriff im 2. Jahr.
Hormontherapie beim Hodenhochstand
Die Erfolgsraten der Hormontherapie beim Hodenhochstand sind wenig konsistent und weisen einen niedrigen Evidenzgrad auf. Obwohl 15 bis 20 Prozent der retinierten Hoden unter einer medikamentösen Behandlung absteigen, kommt es bei 20 Prozent zu einem sekundären Hodenhochstand. Die Hormonbehandlung beim Hodenhochstand verfolgt zwei Ziele:
- Als neoadjuvante Gonadotropine Releasing Hormone (GnRH)-Therapie soll sie den Fertilitätsindex, definiert als Anzahl der Spermatogonien pro Tubulus, verbessern. GnRH stimuliert die Hypophyse (Hirnanhangsdrüse) zur Ausschüttung von luteinisierendem Hormon (LH), welches die testikulären Leydigzellen zur Testosteronproduktion anregt und so den Hodenabstieg in den Hodensack einleitet. Eine vierwöchige präoperative GnRH-Behandlung sollte deshalb zwecks maximaler Transformation der Gonozyten in adulte, dunkle Spermatogonien erfolgen, um den ersten postnatalen Reifungsschritt der Keimzellen zu fördern. Ob hierdurch die Fertilität im Erwachsenenalter tatsächlich verbessert werden kann, lässt sich aufgrund fehlender prospektiver Studien jedoch nicht beweisen.
- Die Einleitung eines Hodenabstieges kann durch eine Therapie mit Human-Chorion-Gonadotropin (HCG) vorgenommen werden. Es regt die Leydigzellen zur Testosteronproduktion an. Durch eine dreiwöchige intramuskuläre Injektion wird eine Verlagerung des Hodens in den Hodensack in 20 Prozent der Fälle erzielt. Nebenwirkungen können sein: Penis- und Hodenvergrößerung, vorzeitige Entwicklung der Genitalbehaarung und aggressives Verhalten der Kinder. Alternativ ist eine GnRH-Monotherapie mit vergleichbarer Erfolgsrate möglich. Eine Kombination beider Hormonpräparate führt nicht zur signifikanten Verbesserung der Ergebnisse.
Standard-Orchidopexie beim Hodenhochstand
Die chirurgische Korrektur der Hodenfehllage stellt den Eckpfeiler der Behandlung des Hodenhochstandes dar. Der Leisten-Zugang gewährleistet im Gegensatz zum Hodensackschnitt die beste Darstellung des Leistenkanals und erlaubt die gleichzeitige Korrektur des häufig bestehenden Leistenbruches. Nach Durchtrenung des Gubernakulums (Abbildung 6) erfolgt eine Orchido- und Funikulolyse (Abbildung 7).
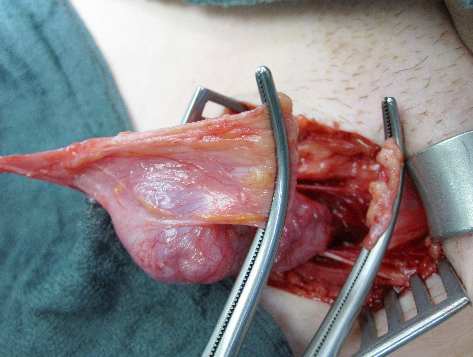
Abbildung 6: Durchtrennung des Gubernakulums
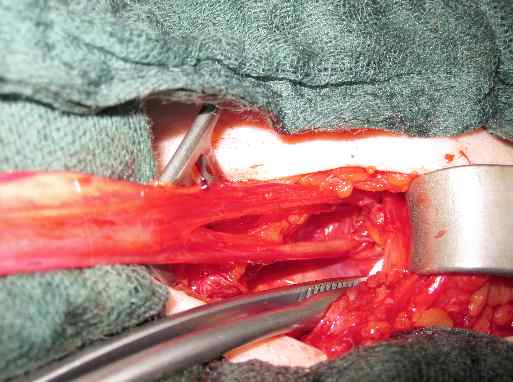
Abbildung 7: Funikulolyse bis zum Peritoneum
Ein offener Processus vaginalis peritonei (angeborener Leistenbruch) wird vom Samenstrang abgelöst und reseziert (Abbildung 8), um eine spannungsfreie Orchidopexie im Skrotum zu erreichen (Abbildung 9).
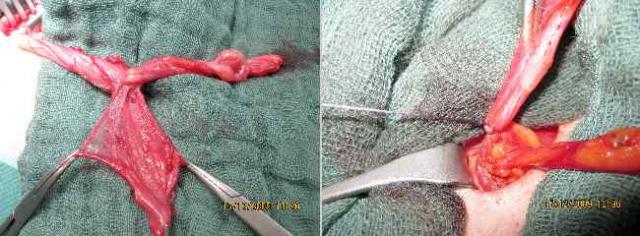
Abbildung 8a und 8b: Resektion des offenen Processus vaginalis peritonei
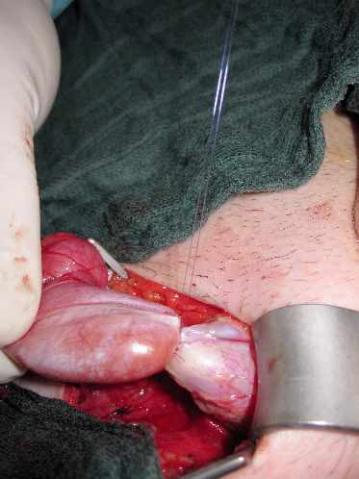
Abbildung 9: Endoskrotale Orchidopexie
Hodenbiopsie beim Hodenhochstand
Es gibt keine Indikation für eine routinemäßige Hodenbiopsie zur Beurteilung des Hoden-Reifungszustandes. Das Risiko einer Durchblutungsstörung mit sekundärer Hodenverkümmerung ist größer als der histologische Informationsgewinn über den Fruchtbarkeitsindex. Nur bei Verdacht auf eine gemischte Gonadendysgenesie (Ovotestis: gleichzeitiges Vorkommen von Hoden- und Eierstockgewebe) oder einen Hodentumor ist sie indiziert.
Laparoskopie und Fowler-Stephens-Operation beim Hodenhochstand
Beim nicht tastbaren Hoden erfolgt eine Laparoskopie zur Identifizierung der Gonade. 10 Prozent der Knaben weisen eine Hodenaplasie auf. Samenstrangrudimente sollten entfernt werden. Findet sich ein erhaltenswerter Hoden, kann in gleicher Sitzung eine sog. Fowler-Stephens-Operation erfolgen. Da der kurze Gefäßstrang des Bauchhodens limitierend ist, werden die Hodengefäße durchtrennt und die Samenleiterarterie erhalten (Abbildung 10).
Der Eingriff sollte zweizeitig vorgenommen werden, um die Ausbildung von Kollateralen zu ermöglichen. Beim einseitigen Vorgehen besteht das erhöhte Risiko eines Gefäßspasmus der Samenstrangarterie, einer testikulären Minderdurchblutung und einer sekundären Hodenatrophie. 3 bis 6 Monate nach der ersten Sitzung erfolgt die Verlagerung des mobilisierten Hodens in den Hodensack (Abbildung 11).
Die Operation ist offen-operativ oder laparoskopisch möglich. Die Langzeitdaten der zweizeitigen laparoskopischen Fowler-Stephens-Operation zeigen eine Atrophierate des Hodens (Hodenverkümmerung) in ca. 17 Prozent und in 83 Prozent einen im Hodensack tastbaren, aber im Vergleich zur gesunden Gegenseite deutlich kleineren Hoden. Es fehlen jedoch nach der Pubertät vorgenommene Fertilitätsuntersuchungen, um die Effizienz dieser chirurgischen Strategie beurteilen zu können.
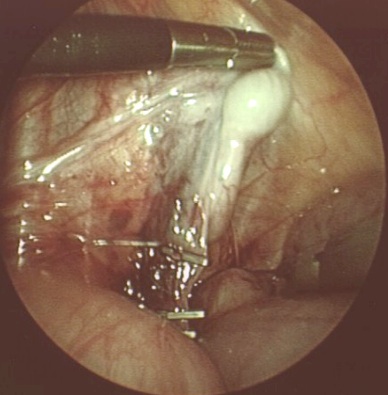
Abbildung 10: Zweizeitige laparoskopische Fowler-Stephens-Operation bei Bauchhoden, 1. OP: Klippung der Samenstranggefäße (mit freundlicher Genehmigung von Prof. Rösch, Regensburg)
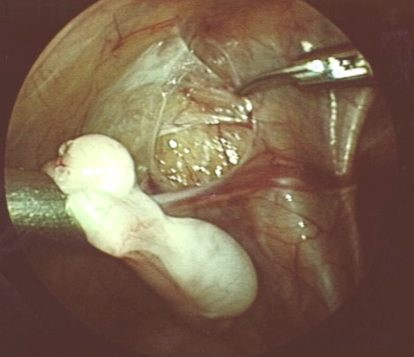
Abbildung 11: Zweizeitige laparoskopische Fowler-Stephens-Operation bei Bauchhoden, 2. OP 6 Monate nach Gefäßklippung: Hodenverlagerung in das Skrotalfach (mit freundlicher Genehmigung von Prof. Rösch, Regensburg)
Autotransplantation beim Hodenhochstand
Dieses Verfahren kann alternativ zur Fowler-Stephens-Operation angewandt werden. Dabei erfolgt eine mikrochirurgische Anastomose der testikulären mit den epigastrischen Gefäßen. Die Erfolgsrate wird mit 84 Prozent angegeben. Im frühen Kindesalter ist diese Technik jedoch durch die kleinen Gefäßdurchmesser limitiert. Es liegen keine Daten mit Langzeitverläufen und Aussagen über postoperative Hodenatrophie- und postpubertäre Fertilitätsraten vor, so dass der Stellenwert dieser Methode unklar bleibt.
Komplikationen bei der operativen Therapie des Hodenhochstandes
Die Komplikationsrate ist unabhängig vom Operationszeitpunkt und liegt zwischen 1 bis 8 Prozent. Hauptrisiken sind
- Rezidive (3 bis 5 Prozent),
- Verletzungen der Samenstranggefäße mit sekundärer Hodenschrumpfung (2 bis 3 Prozent)
- und Durchtrennung des Samenleiters (<1 Prozent).
Postoperative Schwellungen sind häufig. Infektionen und Nachblutungen werden in 0,5 bis 1 Prozent der Fälle beobachtet.
Eine operative Reintervention wegen eines Leistenhoden-Rezidives (erneuter Hodenhochstand) sollte erst nach vollständig abgeschlossener Wundheilung im 6. postoperativen Monat erfolgen. Eine Hormontherapie zur Steigerung der Erfolgsrate ist wegen narbiger Fixierung des erfolglos operierten Hodens sinnlos. Nach Operation eines Bauchhodens wird ein Nachoperation in 17 bis 25 Prozent wegen Rezidiv oder Hodenverkümmerung angegeben und endet häufig in einer sekundären Hodenentfernung.
Schlussfolgerung zum Hodenhochstand
Der Hodenhochstand ist die häufigste männliche Genitalfehlbildung und sollte bis zum 1. Geburtstag erfolgreich behandelt sein. Die Orchidopexie (operative Fixierung des Hodens im Hodensack) stellt dabei das entscheidende Therapieverfahren dar.
Ob eine neoadjuvante GnRH-Behandlung die Fertilitätsprognose vor allem bei bilateraler Hodendystopie verbessern kann, bleibt abzuwarten. Ein beidseitiger Kryptorchismus erfordert einen HCG-Test oder eine Inhibin- Bestimmung. Die Laparoskopie stellt das Verfahren der ersten Wahl zur Diagnose und Behandlung eines Bauchhodens dar. Im Bauchraum gelegene Hoden mit kurzem Gefäßstrang werden einem zweizeitigen laparoskopischen Fowler-Stephens-Verfahren unterzogen.
Die Fertilitätsprognose ist vor allem beim unbehandelten beidseitigen Hodenhochstand eingeschränkt. Das Entartungsrisiko ist 5mal höher als in der Allgemeinbevölkerung und unabhängig vom Behandlungserfolg.


